
Journal of Veterinary Internal Medicine
November/December 2013
https://onlinelibrary.wiley.com/doi/10.1111/jvim.12183
Перевод с англ.: ветеринар - невролог/кардиолог Васильев
Краткое содержание
Доказательства дегенерации межпозвонковых дисков (IVDD) встречаются очень часто и ее распостраненность увеличивается с возрастом. Она имеет много важных последствий, поскольку часто является прелюдией к появлению грыжи диска, которая может травмировать спинной мозг, спинальные нервы или и то и другое. Этот обзор суммирует продвижения в диагностике и лечении IVDD с пятидесятых годов прошлого века, когда были опубликованы первые детальные описания дегенеративных изменений межпозвонковых дисков.Здесь также описываются новые подходы к лечению, ассоциированному с повреждениями спинного мозга и новые методы классификации тяжести поражений, которые разрабатываются в настоящее время.
Дегенерация межпозвонковых дисков является неизбежным проявлением старения и приводит к серии прогрессивных патологических изменений в их структуре. Однако, хотя этот дегенеративный процесс может влиять на биомеханику позвоночного столба, он имеет малую клиническую значимость, если не имеется изменений в контуре диска или выхода его компонентов, часто повреждающих спинной мозг и ассоциированные нервы. Поэтому, основной интерес представляет повреждение, которое возникает вследствие дегенерации, способ его лечения и профилактики. В этом обзоре, мы суммировали механизмы IVDD, подчеркивая вариабельность вариантов грыжи межпозвонковых дисков (IVDH), и ассоциированные механизмы спинального повреждения (SCI), описывая обоснования для современных методов лечения и внедрения достижений в диагностике и лечении, которые разрабатываются в настоящее время.
Процесс IVDD
Нормальный межпозвонковый диск собак состоит из несжимаемого пульпозного ядра, происходящего из эмбриональной хорды, вместе с охватывающим его фиброзным кольцом, которое, вместе с хрящевыми конечными пластинками примыкающих позвонков, ограничивает ядро. Несжимаемая природа ядра, вместе связочным фиброзным кольцом, обеспечивает суставное соединение между позвонками, которое позволяет производить ограниченное движение в любой плоскости и тем, самым, противостоять силе сжатия, направленной вдоль длинной оси позвоночника, которая создается абдоминальными мыщцами и мыщцами, поддерживающими голову
Инициирующим фактором для IVDD у человека, видимо, является потеря диффузионной способности сосудов концевых пластинок позвонков, которые обеспечивают питание пульпозного ядра. Это снижает продукцию внеклеточного матрикса, который преимущественно состояит из гидрофильных протеогликанов и, следовательно, нарушает механические свойства ядра, приводя к вторичным дегенеративным изменениям в фиброзном кольце. Дегенерация кровоснабжения может возникать вследствие различных механизмов у человека, но дегенерация межпозвонковых дисков собак наиболее часто ассоциирована с мультигенными предрасположенностями. Некоторые из них могут вызывать васкулопатию, но, по -видимому, другие, участвующие в этом процессе гены, ассоциированы с предрасположенностью к хондродистрофии.
Таким образом, хотя васкулопатия может быть важным путем в дегенеративном каскаде, преждевременное старение хордовых клеток и замещение их хондроцитоподобными клетками рассматривается как критический механизм у хондродистрофичных собак. Анализ экспрессии генов с помощью ДНК-микрочипов здоровых дисков, в сравнении с дегенеративными дисками собак, наводит на мысль, что супрессия канонической Wnt сигнализации и caveolin-1 экспрессии могут быть критическими шагами к потере популяций хордовых клеток.
Патологические особенности дегенерации межпозвонковых дисков у собак были описаны в классическом исследовании Хансена, опубликованном приблизительно 60 лет назад. Хансен описал 2 отчетливые формы IVDD, каждая типично встречающаяся у различных типов собак. При хондроидной дегенерации, которая встречается преимущественно у хондродистрофичных собак, пульпозное ядро дегидратируется, его клетки дегенерируют и вся структура становится дистрофически кальцифицированной. Эта дегенерация изменяет распределение внутридискового давления, вызывая фокусы механического стресса в фиброзном кольце.
Со временем, этот патологический стресс может привести к разрыву индивидуальных коллагеновых пучков кольца, до тех пор, пока не произойдет окончательное механическое повреждение, которое может возникнуть катастрофически, выпуская дегенеративное ядро. Эта экструзия может произойти в любом направлении, но чаще в дорсальном направлении, вследствие того, что ядро позиционировано эксцентрически в пределах кольца. Хансен ассоциировал этот тип дегенерации с хондродистрофичными собаками и назвал последующую грыжу ядра «тип 1» IVDH.
При фиброидной дегенерации, которая встречается преимущественно у нехондродистрофичных собак, кольцо находится в центре дегенеративного процесса, хотя содержание коллагена в ядре увеличивается, иногда разделяя его на 2 дольки.Волокна кольца отделяются друг от друга, позволяя аккумулироваться тканевой жидкости и плазме. Со временем и при механическом давлении, направленном на ядро (с тенденцией к более дорсальному направлению), этот дегенеративный процесс вызывает утолщение кольца, особенно дорсально. Это может вызывать протрузию кольца в вертебральный канал, где оно может сдавливать спинной мозг или корешки спинальных нервов. Этот тип дегенерации межпозвонковых дисков собак был ассоциирован с нехондродистрофичными собаками и мог вести к грыже диска, названной грыжа Хансена “типа II.”
Более недавние гистологические исследования, хотя, в общем, поддержали оригинальные описания Хансена, говорят о том, что имеется меньшая разница между дегенерацией у хондродистрофичных и нехондродистрофичных собак, чем ранее предполагалось. Специфически, более продвинутые стадии дегенерации фиброзного кольца у нехондродистрофичных собак показали замещение хордовых клеток хондроцитоподобными клетками, что схоже с процессом, который наблюдается у хондродистрофичных собак. С клинической точки зрения, патологическая дифференциация, выполненная Хансеном, в общем, выдержала испытание временем; большинство случаев клинически релевантной IVDH может быть классифицировано в один из 2 типов синдрома. Тем не менее, некоторые случаи IVDH не вписываются ни в одну из двух категорий.
Общим местом является наблюдение оторванных частей кольца в позвоночном канале как хондродистрофичных, так и у нехондродистрофичных собак. Далее, клинические симптомы могут возникать быстро в ассоцииации с типом II IVDH, а хронические клинические симптомы могут быть ассоциированы с типом I IVDH. Далее, имеются разногласия о том, какие собаки могут быть причислены к хондродистрофичным, поскольку кокер спаниели и бигли часто включаются в эту группу, несмотря на отсутствие характерных коротких конечностей.
Последствия IVDD
Происхождение клинических симптомов, ассоциированных с IVDD
Хотя дегенерация межпозвонковых дисков собак встречается очень часто, особенно у хондродистрофичных пород, большинство больных собак не демонстрируют внешних проявлений этого дегенеративного процесса. Когда наблюдаются клинические симптомы, они обычно возникают вследствие воздействия дегенеративного диска на нервные структуры, что может вызывать как боль, так и неврологическую дисфункцию различной степени тяжести. Растяжение волокон дорсальной части фиброзного кольца или дорсальной продольной связки также может вызывать боль активацией богатой ноницептивной иннервации, которую эти структуры содержат.
Когда наблюдаются клинические симптомы, они могут происходить как от (1) растягивании волокон дорсальной продольной связки, что может вызывать боль за счет стимуляции ее ноницептивной иннервации; или (2) от воздействия дегенеративного диска на нервные структуры, что может вызывать как боль, так и неврологическую дисфункцию различной степени тяжести.
Термин IVDH может быть использован для суммирования механизмов, за счет которых дегенеративный диск может вызывать боль и неврологический дефицит, и расшифровывается как локализованное смещение межпозвонкового диска за нормальные трехмерные анатомические пределы диска. Эту патологию можно разделить на 2 подтипа (игнорируя узлы Шморля; эта патология имеет неясное клиническое значение для собак), каждый из которых ассоциирован с различными типами дегенерации межпозвоночных дисков: (1) экструзии дегенеративного ядра (тип I) или (2) протрузии дегенеративного кольца в вертебральный канал (тип II). Эти 2 подтипа подразумевают различные варианты повреждения спинного мозга. Экструзия ядра приводит к смешанной компрессивной и контузионной природе поражения, пропорции каждой из них варьируют в зависимости от обьема материала и скорости, с которой происходит экструзия.
Таким образом, конечный результат может варьировать между почти полной контузией до почти полной компрессии. Наоборот, протрузия кольца обычно, но не эксклюзивно, наблюдается в период от месяцев до лет и, поэтому, вызывает медленно прогрессирующую компрессию смежного спинного мозга. Однако, вследствие движения сегментов позвоночника, она также может дополняться динамической компрессией, при которой компрессия варьирует по тяжести от момента к моменту, в зависимости от непостоянного положения позвонков (Изобр 1)
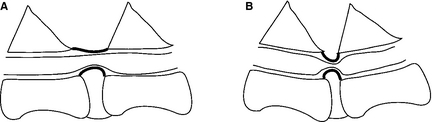
Изобр 1. Линейная диаграмма, иллюстрирующая динамическую компрессию, ассоциированную с протрузией межпозвонкового диска.(А) В состоянии покоя, протрузия дорсального кольца, вызывает слабую компрессию спинного мозга. (В) В течение спинальной дорсофлексии, спинальная компрессия усиливается. Желтая связка, находящаяся дорсальнее спинного мозга, может также способствовать компрессии спинного мозга во время дорсофлексии.
Другие типы IVDH
Увеличение использования магниторезонансной томографии (MRI) для диагностирования поражений позвоночного столба у собак позволила идентифицировать более широкий спектр диск-ассоциированных повреждений спинного мозга. Наиболее значимой из них является подострая экструзия очевидно нормального ядра межпозвонкового диска, предположительно связанная с супрафизиологическим, механическим стрессом во время выполнения спортивных упражнений.Часть ядра с взрывной скоростью выстреливается из кольца и его смещение может легко наблюдаться на MRI.Этот тип экструзии диска также иногда может ошибочно отнесен к грыже межпозвоночного диска “тип III, но этот термин не должен использоваться, поскольку такие случаи не показывают наличие предшествующей дегенерации диска. Вместо этого, Хансен использовал термин травматический пролапс диска. Поражение спинного мозга. вызванное этими взрывными поражениями, широко варьирует, но может быть очень тяжелым (см ниже).
Схоже с этим, но отчетливо различающееся, поражение, описанное в шейном регионе у собак, при котором материал выглядит гиперинтенсивным на T2WMRI сканах, наблюдается вентральнее спинного мозга (Изобр 2). Рентгенологическая интерпретация поддерживает хирургические находки в некоторых случаях, является то, что материал экструдированного гидратированного ядерного материала и может быть ассоциирован с умеренной спинальной компрессией; тяжесть ассоциированной SCI вариабельна.
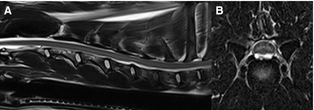
Изобр 2. T2WMRI изображения от собаки с острым началом неамбулаторнорного тетрапареза и атаксии, локализованной в шейном отделе спинного мозга. (А) Сагиттальные изображения выявили фокальную вентральную экстрадуральную компрессию спинного мозга дорсальнее C5–C6 дискового пространства с ассоциированным сужением дискового пространства и частичной потерей нормального T2 ядерного сигнала.(В) Поперечное изображение через C5/C6 межпозвоночный диск, иллюстрирующее гиперинтенсивный материал вентральнее спинного мозга с изображением типа « чайка».Эти MRI особенности характерны для экструзии гидратированного пульпозного ядра, которая была подтверждена хирургически.
Контузия
Контузионное повреждение наиболее понятно из всех механизмов повреждений, ассоциированных с IVDH, поскольку его относительно легко воспроизвести в лаборатории. Первой моделью (кстати, опробованной на экспериментальных собаках) был метод ударного повреждения после падения, при котором определенная масса падала с определенной дистанции, воздействуя на спинной мозг, и затем удалялась. Этот метод был значительно усовершенствован в последние десятилетия и сейчас моделирование основано на повреждении спинного мозга, контролируемое компьютером, почти исключительно с использованием грызунов, при котором скорость, сила и продолжительность контузии варьируются, и которое также включает обратную информацию, чтобы обеспечить воспроизводимость силы и удара и постоянность повреждения.
Это моделирование на лабораторных животных обеспечивает базовую информацию, на основании которой делаются выводы о биохимических и клеточных процессах, которые наблюдаются при SCI у клинических пациентов и обозреваются во многих базовых научных, медицинских и ветеринарных публикациях. Несущественное, локализованное аксональное повреждение может быть выявлено немедленно после контузии спинного мозга и имеется доказательство сосудистого повреждения, включая нарушение гемато-спинального барьера, со слабовыраженным структурным повреждением при такой травме.
После этого первичного повреждения, в течение нескольких последующих дней (приблизительно 7) развивается вторичное повреждение, запущенное немедленными сосудистыми (вазоконстрикция плюс экстравазация клеток и плазмы в нейропиль) и клеточными реакциями, которые вызывают прогрессирующее повреждение ткани с кульминирующей потерей нейронов, олигодентроцитов и аксонов и окончательным замещением разрушенной ткани тканевой жидкостью, реактивными астроцитами или и тем и другим. Механизмы, лежащие в основе этого вторичного повреждения были установлены в предыдущие 2 десятилетия лабораторными исследованиями и это дает основание для надежды, что лечение будущего может ослаблять прогрессирующую деструкцию ткани спинного мозга, что, в настоящее время, неизбежно следует за тупыми травмами спинного мозга.
Ключевым патологическим результатом контузионного повреждения является поступление кальция в тела нейронов, аксонов, астроцитов и олигодендроцитов. Это активирует широкий круг энзимов, таких как calpains и caspases, которые активируют аутодеструктивные механизмы и могут приводить к апоптозу и некрозу. Конечные результаты этого процесса тоже иллюстрируются в исследованиях, проведенных у эутаназированных ветеринарных пациентов. Свободные радикалы, выпускаются после энзиматической деструкции митохондриальных мембран, активированной микроглии и активации нейронной синтазы оксида азота и вызывают прогрессивное повреждение клеточных мембран и дополнительные циклы смерти клеток.Активированные сигнальные пути воспаления вызывают нарушение тонуса сосудов и инфильтрацию воспалительными клетками нейропиля.
Активация микроглии, по- видимому, является важным событием у собак с естественно встречающимся SCI, и выпуск цитокинов в этой клеточной популяции может быть важным в управлении врожденными воспалительными реакциями. В частности, интерлейкин -1 (IL-1),фактор тканевого некроза (TNFα), и оксид азота участвуют в повреждении нейронов и олигодендроцитов; однако, имеется также доказательство, что микроглия также может играть защитную роль при SCI. К примеру, микроглия также продуцирует трансформирующий фактор роста (TGFβ), который имеет нейропротективные эффекты и имеется прямое доказательство из invivo исследований, что трансплантация активированных макрофагов может быть ассоциирована с регенерацией аксонов и функциональным улучшением.
Нейтрофилы накапливаются в ранних стадиях и прямо вызывают клеточную гибель, поскольку они продуцируют свободные радикалы, которые разрушают клеточные мембраны. За ними следуют лимфоциты, которые становятся аутореактивными, имеющие целью ранее скрытые антигены центральной нервной системы. С другой стороны, имеется также доказательство полезных эффектов Т-клеточно -обусловленных ответов на аутоантигены из производных миелина, что говорит о тонком балансе между повреждением и защитой, которые могут зависеть от факторов, которые пока не полностью понятны.
Поступление кальция первоначально зависит от клеточной деполяризации (вследствие прямого повреждения), способствующей входу натрия, который затем обменивается на кальций,особенно в аксонах. Клеточная деполяризация также способствует выпуску возбуждающих нейротрансмиттеров, главным образом, глютамата, который может, в свою очередь, способствовать входу кальция при помощи NMDA рецепторов. Глютамат в избытке является токсичным при этом процессе, что называется эксайтотоксичностью. Разрушение олигодендроцитов ( которые особенно уязвимы, вследствие большой площади их мембран и NMDA рецепторов) будет вести к демиелинизации аксонов, которая, в свою очередь, делает их более чувствительными к деструкции.
Итоговый гомеостаз устанавливается ответами астроцитов, что формирует новые глиальные мембраны и восстанавливает гемато-спинальный барьер. Конечным результатом является формирование глиальных рубцов, состоящих из реактивных астроцитов плюс значительное отложение протеиногликанов хондроитина сульфата и кератина сульфата, все они являются сильными ингибиторами регенерации отростков аксонов, таким образом, предотвращая восстановление поврежденных соединений в поврежденной зоне.
Как правило, неповрежденные ткани (если они остались) локализуются на периферии спинного мозга. Это наводит на мысль, что более центральные регионы более чувствительны к контузионному повреждению, вероятно, вследствие того, что кровеносные сосуды в сером веществе более легко повреждаются и внутренняя часть белого вещества находится в зоне водораздела между кровью, доставляемой периферическими артериями и кровью центральной вентральной артерии. Имеется также доказательство, что серое вещество центральной нервной системы имеет более выраженные энергетические потребности, чем белое вещество, делая его более чувствительным к нарушению кровоснабжения, ассоциированного с повреждением.
Клинические симптомы контузии
Типично, контузионное повреждение ассоциировано с быстрой потерей неврологической функции, наблюдающееся в течение от нескольких секунд до нескольких минут. Однако, при ассоциации с IVDH, клинически наблюдаемые проявления могут встречаться в течение периода от нескольких минут до нескольхих дней, в зависимости от скорости экструзии ядра.Локализация поражения обычно нетрудно устанавливается, на основании типичного набора клинических признаков, которые ожидаются при поперечной миелопатии в специфической локализации.В некоторых острых случаях клиническая картина может быть осложнена спинальным шоком, при котором спинальные рефлексы, каудальнее тяжелого острого поражения, могут быть сниженными (иногда в течение нескольких дней), хотя это зависит от вида (и используемого определения).
Эта клиническая картина может создавать путаницу, относительно точной локализации, поскольку снижение рефлексов конечности наводит на мысль о поражении в пределах спинального утолщения. Для примера, после тяжелого грудопоясничного повреждения сгибательные рефлексы тазовых конечностей у собак могут быть сниженными или отсутствовать в течение до 24 часов. Внимательное рассмотрение кожнотуловищного рефлекса (панникулюса) может обеспечить точную локализацию поражения в таких случаях. Изменения в координации рефлекса мочеиспускания, которые встречаются в течение первых нескольких недель после грудопоясничного SCI, иногда также являются отражением разрешения спинального шока.
Миеломаляция может распостраняться краниально и каудально от эпицентра повреждения и в некоторых случаях будет подниматься и опускаться на расстояние нескольких сегментов, что может быть фатальным. Она наиболее распостранена после тяжелой грудопоясничной контузии и может наблюдаться примерно у 10% собак, у которых имеется полная потеря болевой чувствительности с тазовых конечностей. Механизмы, вследствие которых развивается восходящая миеломаляция, неполностью понятны, предполагается, что миеломаляция развивается вследствие ишемии,вероятно, происходящей вследствие спазма и тромбоза сосудов.
Типичные клинические симптомы восходящей и нисходящей миеломаляции включают потерю изначально нормальных спинальных рефлексов, аключая сгибательные рефлексы на грудных и тазовых конечностях, респираторный дистресс и, в конце концов, во многих случаях смерть, как результат респираторного паралича. Угрожающие симптомы ее развития, такие как сниженная температура тела и восходящий cutoff, кожнотуловищного рефлекса (панникулюса), могут быть выявлены в течение примерно 2 дней после повреждения. При этом состоянии не существует лечения, а собаки с дистрессом должны быть эутаназированы.
Компрессия спинного мозга
Хотя компрессия спинного мозга часто наблюдается как у людей, так и у животных, существует на удивление мало лабораторных исследований этой патологии. Давно известно, что хроническая компрессия приводит потере аксонов с признаками дегенерации Валериана в сегментах дистальнее поражения, и, в общем, представляется, что повреждение белого вещества более заметно. Механизмы, вследствие которых это происходит, еще не выяснены, но считается, что они вызваны плохим кровотоком за счет повышения давления в пределах границ мягкой мозговой оболочки. Однако, также имеются доказательства, полученные из in vitro исследований, что слабая компрессия может вызывать обратимый блок проведения, вероятно, обусловленный изменениями в мембранной проницаемости. Пролонгированная компрессия спинного мозга у экспериментальных животных ассоциирована с демиелинизацией.
В 1969 г Райт и Палмер описали гистологическую картину спинного мозга, который испытывал компрессию в течение длительного периода времени, и пришли к выводу, что нарушение венозного дренажа было ответственно за плохой кровоток через очаг поражения. В более позднем экспериментальном исследовании у собак, al-Mefty et al сообщили, что эпицентр поражения был в водоразделе отделов спинного мозга, в соединении между регионом, снабжаемым периферическими артериями и вентральной спинальной артерией. Поэтому, в этой модели, наиболее поврежденной зоной, вероятно, является периферия серого вещества, но при этом повреждается как серое, так и белое вещество.
Однако, в этой модели использовалось дополнительное увеличение давления, для того, чтобы продуцировать долговременную компрессию, и был вовлечен шейный регион, наводя на мысль, что динамическая компрессия также может играть важную роль. И наоборот, в других моделях демонстрировалась прогрессивная потеря серого вещества, в зависимости от продолжительности и выраженности компрессии, наводя на мысль о том, распределение повреждения при хронической компрессии включает как серое, так и белое вешество. Оценка патологического материала от собак с хронической протрузией диска поддерживает эту точку зрения.
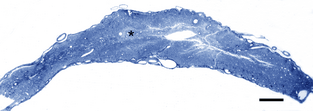
Изобр 3 Поперечный полутонкий срез через регион хронической спинальной компрессии, иллюстрирующий большую потерю серого вещества, * показывает единственный остающийся регион серого вещества (дорсальный рог). Также имеется существенная потеря белого вещества и целостности аксонов. Голубой толуидин, шкала: 500 мм.
Клинические симптомы компрессии спинного мозга
Компрессия спинного мозга, вызванная типом II IVDH, классически ассоциируется со слабо выраженным началом клинических симптомов. Владельцы типично сообщают о потере функции, встречающейся в течение периода от недель до месяцев, часто с периодами внезапного острого ухудшения состояния. Симптомы зависят от локализации поражения и могут включать дефицит как серого, так и белого вещества и обычно прогрессируют очень медленно. Симптомы боли могут отмечаться владельцами, хотя они, вероятно, не отражают компрессию спинного мозга (поскольку паренхима спинного мозга не содержит болевых рецепторов), но могут отражать стимуляцию болевых рецепторов фиброзного кольца или возникают вследствие компрессии нервов.
Поражения спинномозговых нервов
Грыжа межпозвонкового диска собак также может вызывать повреждение периферических нервов, вследствие близости спинальных нервов к межпозвоночным дискам. Хотя контузионные повреждения нервов могут встречаться как результат поражений межпозвоночных дисков, эти эффекты самопроизвольно исчезают, в то время как компрессия является более частой и более трудной для лечения. Существуют 2 основные анатомические локализации, в которых наблюдается компрессия нервов — позвоночный канал в поясничнокрестцовом регионе и позвоночные отверстия в любом межпозвоночном пространстве. Нервы в межпозвонковых отверстиях чувствительны к компрессии, если грыжа межпозвоночного диска локализуется скорее латерально, чем дорсолатерально и иногда может сдавливать нерв латеральнее отверстия. Спинальные нервы часто сдавливаются при типе I TL IVDH и это является вероятным источником боли.
В шейном или поясничнокрестцовом регионах латерализованные экструзии дисков могут вызывать хромоту или боль в конечности из-за компрессии нервов. В поясничнокрестцовом регионе, один или несколько нервов в cauda equina могут быть сдавлены в пределах позвоночного канала, вызывая различные клинические симптомы, ассоциированные с дефицитом функции каудальных поясничных, крестцовых и каудальных нервов. Латерализованные поражения межпозвонковых дисков собак также могут встречаться в поясничнокрестцовом регионе и животные с такой патологией обычно чаще демонстрируют хромоту, чем типичный неврологический дефицит, которая может привести владельцев на консультацию к ортопеду. Компрессия нервов может очень болезненна и этот тип поражения должен подозреваться у животных, которые демонстрируют резкую боль, даже без наличия других локализованных симптомов.
Дифференциальный диагноз
Вариабельность начала и прогрессирования клинических симптомов, относящихся к IVDH, означает, что часто имеется длинный перечень возможных диагнозов для заболевших животных.Хотя IVDD наблюдается в пределах позвоночного столба, локализации, в которых IVDH выявляется как клиническая проблема относительно ограничены. В грудопоясничном регионе примерно 75-80 % острой IVDH наблюдается между T11и L1 дисковыми пространствами и схожая пропорция острой щейной IVDH локализуется от С2 до С4. Хроническая IVDH наиболее часто наблюдается в каудальном шейном, грудопоясничном соединении и на уровне L7/S1.Грудопоясничный регион, как предполагается, более чувствителен, поскольку он лежит в месте соединения между имеющим массивную мускулатуру (и, поэтому, относительно ригидным) поясничным регионом и ригидной грудной клеткой. Кроме того, имеются изменения в ориентации суставных фасеток синовиальных суставов в пределах этой зоны.
Предрасположенность каудального шейного региона к хронической IVDH связана с увеличенными ротационными усилиями, которые могут быть приложены к межпозвонковым дискам, благодаря ориентации суставных фасеток. Поясничнокрестцовый регион может быть чувствителен вследствие того, что он находится в центре локомоторных усилий, передающихся от таза к позвоночному столбу, кроме того в этих межпозвонковых пространствах также имеется высокая встречаемость врожденных деформаций, которые ассоциированы с симптоматическими поражениями межпозвонковых дисков.
В общем, могут быть идентифицированы 3 синдрома, ассоциированные с симптоматической IVDD: боль, острая и хроническая атаксия и парез. Различные диагнозы для каждого из них суммированы в табл 1. Для животных, представленных с очевидными симптомами боли в позвоночном столбе, имеется много возможных альтернативных причин, включая абдоминальные заболевания (поскольку животные с абдоминальной болью будут часто напрягать свои мыщцы брюшной стенки таким же образом, как и животные со спинальной болью), различные воспалительные, инфекционные или неопластические заболевания (которых много) любой осевой мышечноскелетной структуры. Сужение круга возможных дифференциальных диагнозов зависит от внимательного обследования, имеющего целью точно локализовать место поражения и обьективного использования данных истории болезни.
Для животных, представленных с острым парезом или атаксией наиболее частыми дифференциальными диагнозами являются поражения, которые будут вызывать нестабильность позвоночного столба, такие как патологические или травматические переломы, ишемическая миелопатия и миелит. Опухолевые поражения могут вызывать острое начало клинической симптоматики в позвоночнике поскольку, хотя опухолевые процессы прогрессируют медленно, ассоциированные патологические переломы или сосудистые нарушения встречаются остро. В частности, опухоли с высоким митотичеким индексом могут быстро увеличиваться в размере и приводить к острому тромбозу или разрыву сосудов спинного мозга или их разрыву.
Существует много других возможных причин для возникновения острого пареза или атаксии (см Табл 1), существует также потенциальная путаница при поражениях периферической нервной системы из-за дефицитов, ассоциированных со спинальными утолщениями (поскольку они могут вызывать клинические симптомы вялого пареза, потери сенсорных реакций или и тех и других).
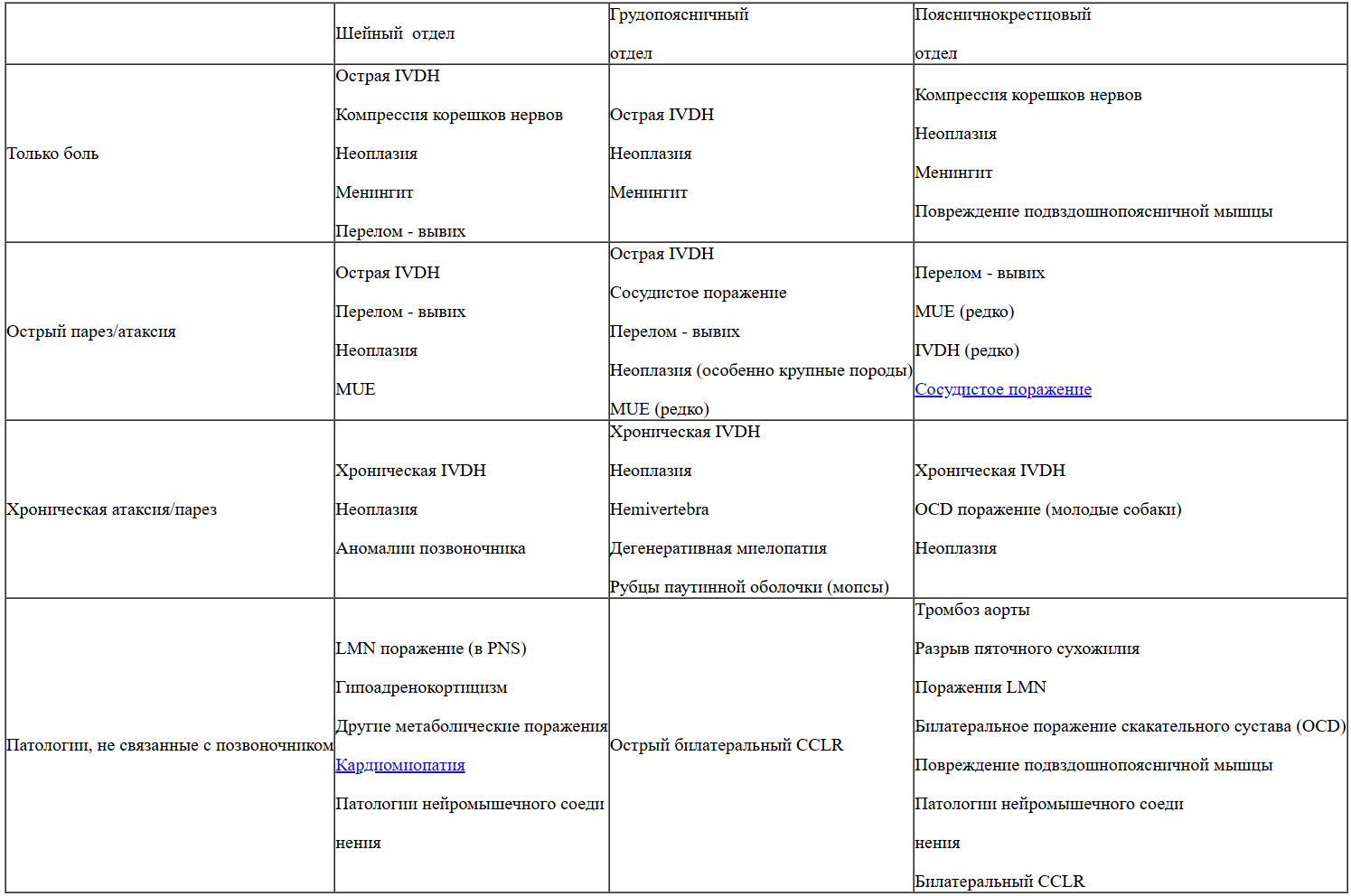
Табл 1. Перечень хорошо диагностируемых причин специфической клинической картины, которая может быть вызвана грыжей межпозвонкового диска собак
CCLR, разрыв краниальной крестовидной связки; IVDH, грыжа межпозвоночного диска; LMN, нижний двигательный нейрон; MUE, менингоэнцефаломиелит неизвестной этиологии; OCD, рассекающий остеохондри ; PNS, периферическая нервная система; Junctionopathies, нарушение передачи импульса с нерва на мыщцу; Hemivertebra, врожденное недоразвитие половины позвонка
Для животных,представленных с хроническим парезом или атаксией, основными дифференциальными диагнозами являются другие компрессионные поражения, особенно неоплазия, или дегенеративные состояния, поражающие центральную нервную систему, такие как дегенеративная миелопатия. Трудности могут возникать в дифференциации дегенеративной миелопатии от типа II IVDH, особенно у среднего возраста немецких овчарок, поскольку отдельные особи могут одновременно страдать обоими заболеваниями.В таких случаях, если при выполнении продвинутых технологий диагностики выявляется компрессия спинного мозга, ассоциированная с грыжей диска II типа, может быть полезным тестирование на SOD1 мутацию для того, чтобы установить, имеет ли собака также риск развития дегенеративной миелопатии.
Для случаев, когда имеется грыжа диска II типа и риск дегенеративной миелопатии одновременно, лечение с применением кортикостероидов может быть также полезным, поскольку это будет, по меньшей мере частично, ослаблять клинические симптомы, ассоциированные с компрессией спинного мозга, но это лечение не даст эффекта при дегенеративной миелопатии. Высокая частота встречаемости мутации SOD1 у нормальных собак некоторых пород может сделать интерпретацию генетических тестов единственным методом диагностики в отсутствие возможности визуализации спинного мозга.